“.I would rather have questions that cannot be answered than answers that cannot be questioned”
(Richard Feynman)
הקדמה
על פי ארגון הבריאות העולמי (WHO) מספר החולים בדמנציה ברחבי העולם עומד על מעל חמישים וחמישה מיליון אנשים, ומעריכים כי המספר ישתלש עד שנת 2050. מחלת הדמנציה נמצאת בעשירייה המובילה של גורמי המוות בעולם, 60-70% מהמקרים בשל מחלת אלצהיימר.
למרות שרוב מקרי האלצהיימר מופיעים בצורה אקראית, לפני כמה שנים גילו מוטציה בשלושה גנים המתבטאים בהרבה מהמקרים:(1APP) (PSEN2) (PSEN) . גילוי שלושת הגנים היה הביסוס לתאוריה הרווחת על תפקידם המרכזי של הבטא עמילואידים בפתולוגיה של אלצהיימר, ובעקבות כך פותחו תרופות להפחתת הבטא עמילואידים. אבל עם המחקרים החדשים הנעשים בתחום האלצהיימר מתגלים גורמים אחרים למחלה.
ידועים לנו כמה גורמי סיכון העלולים לקדם אלצהיימר גם ללא הופעת המוטציה הגנטית – עודף משקל, יתר לחץ דם, וחוסר שינה (שכן נמצא כי בשינה המוח מקדם פינוי פסולת כגון עמילואיד בטא וחלבונים אחרים). על סמך ממצאים אלה שיערו החוקרים כי התכונות המשקמות של שינה עשויות להיות קשורות לפינוי גלימפטי (Galymphatic system) מוגבר של תוצרי פסולת מטבולית המיוצרים על ידי פעילות עצבית במוח ער.
עוד גורם סיכון הוא תזונה לקויה בשל ציר המוח-מעי (GBA), המקשר בין פעילות המעי והמוח. מחקרים אחרונים מתארים את חשיבות המיקרוביוטה של המעי על המוח ונמצא כי האינטראקציה בין המיקרוביוטה לבין GBA היא דו-כיוונית, כלומר באמצעות איתות מהמיקרוביוטה של המעי אל מוח ומהמוח אל המיקרוביוטה של המעי נעשים שינויים עצביים ומטבוליים.
גם חוסר פעילות קוגניטיבית מהווה סיכון לפיתוח דמנציה, בשל תהליך ניווני.
אבל למרות כל אלו, המנגנון הפתו-פיזיולוגי של האלצהיימר עוד לא לגמרי ברור. אנחנו כן יודעים שבגיל השלישי מנגנוני החיסון מוחלשים, מערכת העצבים לעיתים שחוקה ומנגנון נטרול הרדיקלים החופשיים במוח ירוד, לכן המוח רגיש יותר לנזק חמצוני. אצל הרבה מבני הגיל השלישי נראה שהתזונה מתדלדלת מכל מיני סיבות, יכולת הספיגה יורדת ואיתה גם הובלת החומרים לאזור הזקוק להם. ישנה גם ירידה משמעותית בנירוטרנסמיטור אציטילכולין, החיוני ללמידה וקשב.
אז אם גורמי הסיכון למחלה מערבים מערכות נוספות מלבד המוח, עולה השאלה האם אפשר להגיד שהמחלה הנוירודגנרטיבית מסתמכת כולה על הצטברות הבטא עמילואידים במוח? מחקרים חדשים מפריכים את מה שידענו על הפתולוגיה של אלצהיימר עד כה, ואת יעילות התרופות שנוצרו בעקבות כך.
נקודת מבט הוליסטית
מחלת האלצהיימר נחקרה במשך עשורים בעיקר תוך התמקדות בהצטברות של β-amyloid. עם זאת, מחקרים עדכניים מצביעים על כך שהשינויים המולקולריים הקשורים במחלה מתחילים שנים רבות לפני הופעת הסימפטומים. מעורבים בהם גורמים מערכתיים הכוללים דיסביוזיס של המיקרוביום, תהליכי דלקת כרוניים נמוכי עוצמה, ירידה בפעילות מיטוכונדריאלית, ופגיעה במנגנוני סילוק רעלים נוירונליים, בעיקר דרך מערכת הגלימפה המוחית.
טיפול בצמחי מרפא במחלת אלצהיימר יכול לאגד חיזוק מחסום דם-מוח (BBB), איזון ציר המעי-מוח (GBA), ותמיכה בפינוי גלימפטי. זו גישה המציעה שאלצהיימר אינו רק תוצאה של הצטברות חלבונים, אלא ביטוי של קושי בויסות עצבי, חיסוני ומטבולי.
מטבוליטים משניים כגון פלבנואידים, apigenin, חומצה רוזמרינית, קרוטנואידים ואלקלואידים נוירואקטיביים, הוכחו כבעלי השפעה נוירופרוטקטיבית.
צמחים נוספים בעלי אפיניות למערכת העצבים מראים יעילות במצבים שונים של המחלה. בספרה, ד״ר מינה פארן מפרטת כמה הג׳ינקו (ginkgo biloba) חשוב לאוכלוסיה מזדקנת.
בשנים האחרונות נעשו מחקרים על ההשפעה המיטיבה והמונעת של המרווה הסינית (salvia miltiorrhiza), צמח בעל היסטוריה רפואית של מעל אלפיים שנים בסין. הממצאים משמעותיים בשל ההטבה במצב חולי אלצהיימר, ולא רק מניעה או האטת קצב המחלה.
חומצות סלבינואלית A/B משפיעות על סיגנלים בין תאים, איתותים המעורבים בדלקת, אפופטוזיס ואטופגיה. הן נוגדות חמצון עוצמתיות ומדכאות ביטוי של ציטוקינים דלקתיים ברקמת המוח. חומצה סלבינואלית B מסוגלת להגביר ביטוי חלבונים neprilyisin, IDE – שתפקידם לפרק עודפי AB במוח ואינסולין בגוף, לכן במצב של תנגודת לאינסולין נוכל לראות גם עליה של כמות AB במוח.
מחקרים קליניים הראו שחומצה סלבינואלית B משפרת זיכרון ולמידה ומגנה על תאי עצב.
תמצית המרווה הסינית הפחיתה סטרס חמצוני והראתה שיפור ברמות האנרגיה של המערכת הכולינרגית. בעלת פעילות אנטי דלקתיות עם אפיניות לרקמת המוח, בניסויים על תרביות תאי עצב הראתה תמצית הצמח קידום ניורוגנזה.
מחקרים הראו כי מרווה (Salvia miltiorrhiza) יכולה להקל על תפקוד קוגניטיבי לקוי של חולי אלצהיימר (1).
רוצים לשמוע עוד על טיפול הוליסטי ממוקד בצמחים?
מוזמנים לכנס עיוני גדול ומרתק בנושא טיפול באלצהיימר דמנציה ופרקינסון באמצעות צמחי מרפא.
התרופות בשוק
בשנים האחרונות ה-FDA אישרו תרופות חדשות שתפקידן להוריד את רמות הפלאקים העמילואידים.
למשל התרופה leqembi-Lecanumab, הנקשרת לעמילואידים ומעודדת פינוי שלהם ע״י תאי מיקרוגליה. התרופה הוכיחה האטה של כ- 27% בהתדרדרות הקוגניטיבית אצל חולים בשלבים מוקדמים של המחלה בלבד.
מערכות בריאות במדינות שונות וביניהן בריטניה, דחו את התרופה בטענה שהממצאים החיובים לא מספיק משמעותיים כדי להצדיק את המחיר הגבוה של התרופה, ואת תופעות הלוואי הרציניות הכוללות בצקת מוחית, דימומים, טשטוש ראייה וסחרחורות (2). למעשה ישראל היא אחת המדינות המעטות שאישרה את השימוש בתרופה.
עוד תרופה שאושרה לשימוש לאחרונה, היא Aducanumab המאטה את קצב ההתדרדרות הקוגניטיבית בחודשים ספורים, ורלוונטית רק בשלבי המחלה המוקדמים.
תרופות נוספות שהיו בשימוש במשך השנים הן מסוג מעכבי האנזים אציטילכולין אסטראז, ותרופות אגוניסטיות לקולטני MNDA המווסתות גלוטמט.
מטרת מרבית מהתרופות היא להוריד את כמות הבטא עמילואידים ובכך להפסיק את התדרדרות המחלה, בינתיים לא נרשמו מקרי הצלחה בתחום זה.
סקירת מחקר
בין המאמרים הראשונים שהציגו את הטענה שמחלת אלצהיימר לא נגרמת על ידי פלאקים של בטא עמילואידים בלבד, היה מאמר (3) שהתפרסם ב-PNAS ב- 9 בינואר שנת 2007 על ידי Jie Shen:
The presenilin hypothesis of Alzheimer’s disease: Evidence for a loss-of-function pathogenic mechanism
החוקרים הציגו ניסוי בעכברים שבו היה ניוון משמעותי של קליפת המוח, אובדן סינפסות ותפקוד קוגניטיבי ירוד גם בהיעדר בטא עמילואידים.
מחקר עדכני ומהפכני (4) שהתפרסם במגזין Brain בשנת 2024 על ידי Jesus Abanto:
Increases in amyloid-β42 slow cognitive and clinical decline in Alzheimer’s disease trials
by Jesus Abanto, 11 September 2024, Brain
מצא שירידה בכמות הפלאקים של בטא עמילואידים לא הראתה שיפור במצבם של חולי האלצהיימר.
לעומת זאת, עליה של חלבון במוח בשם (amyloid beta 42 (Aβ42, גרם להאטה התדרדרות הקוגניטיבית בחולי אלצהיימר ויתכן כיוון לתרופה חדשה.
החוקרים מאוניברסיטת סינסינטי גילו שעליה בחלבון המסוים במוח הראה שיפור קוגניטיבי, וניסו להבין מה המנגנון האחראי לעליה ברמת החלבון במוח, ואיך הוא קשור לתרופות הקיימות לטיפול באלצהיימר.
במשך שנים התאוריה הרווחת לפתו-פיזיולוגיה של אלצהיימר הייתה הצטברות של אותם בטא עמילואידים בתאי העצב. המחקרים החדשים שנעשים מגלים לנו שכנראה הבטא עמילואידים הם לא הבעיה. התברר לחוקרים שרוב התרופות לא רק הורידו את רמות הבטא עמילואידים, אלא גם העלו במקריות את רמות החלבון (Aβ42) 42-amino acid isoform .
החוקרים שיערו ומצאו שכמות תקינה של Aβ42, אותו חלבון שהתרופות לאלצהיימר גרמו לעליה שלו, הכרחית לבריאות נוירונים, ודווקא הפחתת כמות החלבון הזה היא הגורמת לאלצהיימר, ולא הצטברות העמילואידים.
לפי המחקר הטרנספורמציה של החלבון המועיל Aβ42 לפלאקים עמילואידים קורה במצב פיזיולוגי תקין, כשהמוח מגיב לסטרס מטבולי, ביולוגי או דלקתי, זאת אומרת תגובה יום יומית בעולם המודרני.
ד״ר אלברטו אספאי (Espay) פרופסור לנוירולוגיה באוניברסיטת סינסינטי מרחיב ואומר:
״לרובנו יש פלאקים של בטא עמילואידים במוח שלנו ככל שאנו מזדקנים, ולמרות זאת, רק אצל מעטים מאתנו הפלאקים יפתחו דמנציה״.
אז למעשה, התרופות שנועדו להוריד את רמות הבטא עמילואידים הראו שיפור מסוים בגלל שעזרו להעלות את רמות החלבון Aβ42 בנוזל המוח והשדרה (CSF).
המחקר מבהיר שהבטא עמילואידים עצמם הם לא גורם ישיר למחלת אלצהיימר, אלא המצב שבו המוח מייצר יותר מדי בטא עמילואידים במטרה להגן על עצמו מרעלנים, שינויים ביולוגים או סטרס מתמשך. ועל חשבונו אין יצור מספיק של החלבון Aβ42. כשערכי חלבון זה נמוכים מאוד, אז מתחילים סימפטומים של דמנציה.
החוקרים סקרו מעל 26000 מחקרים קליניים של טיפול באלצהיימר ומצאו שככל שרמת החלבון Aβ42 הייתה גבוה יותר כך התדרדרות המחלה הייתה איטית יותר. יותר מכך, החוקרים מאמינים ששימוש בתרופות הקיימות להפחתת עמילואידים, בלי שעולה רמת החלבון המועיל Aβ42, יכול ליצור רעילות ולגרום למוח להתכווץ בקצב מהיר יותר.
כעת עובדים החוקרים על תרופה שתעלה את רמות החלבון המועיל בלי להוריד את רמות הבטא עמילואידים.
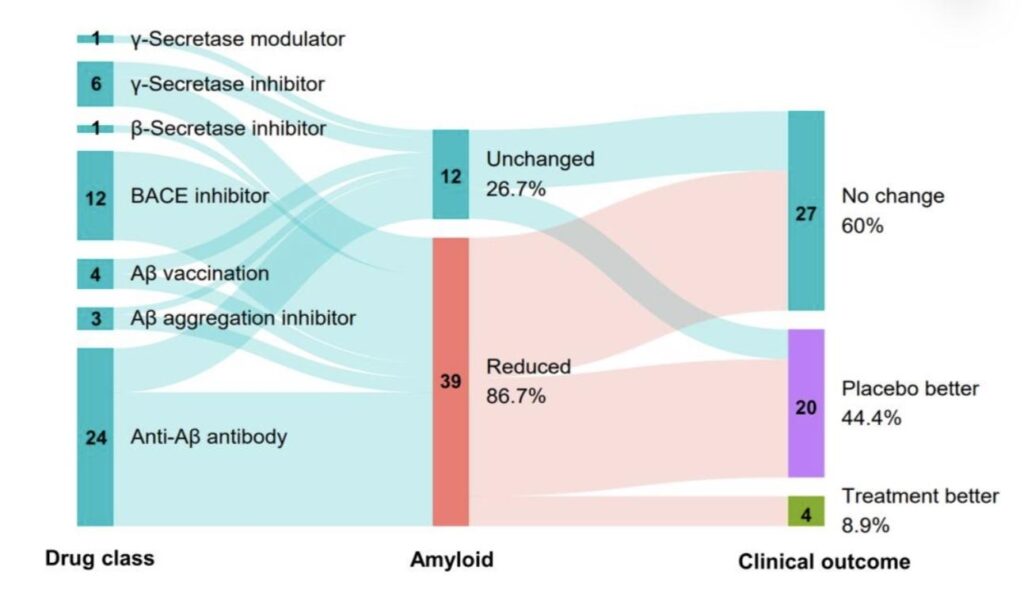
התמונה ממחישה את האפקט התרפויטי של התרופות הקיימות לאלצהיימר במחקרים קליניים, ההשפעה שלהן על בטא עמילואידים והתוצאות.
אפשר לראות שפחות מעשרה אחוזים הראו שיפור בעקבות הטיפול. התרופות מצליחות להוריד את רמת הבטא עמילואידים ב- 86.7% מהמקרים, ולמרות זאת אין כמעט השפעה קלינית חיובית במצב המטופלים בפועל.
מסקנות
הממצאים מהווים תפנית בהבנת הפתו-פיזיולוגיה של מחלת האלצהיימר ודרכי הטיפול בה. ייתכן שבמקום עודף או הסתיידות של חומרים קיימים, המחלה היא מצב של חוסר, מה שגורם לדרך הסתכלות אחרת על הטיפול הצמחי ועל בחירת החומרים המתאימים לטיפול. יש צורך בהמשך מחקר מדעי והרבליסטי בתחום.
עם התקדמות הרפואה והמדע, תוחלת החיים ממשיכה לעלות, והתמודדות עם ההשלכות של הזדקנות האוכלוסייה הופכת לאתגר מרכזי. יש המתארים את הגיל השלישי כ”אור הדמדומים” של החיים, תקופה המוקדשת להכלה, הנאה ושהייה בקרב בני משפחה. יחד עם הארכת החיים, גובר גם החשש ממחלות ניווניות, והתקדמות המחקר משנה תדיר את דרכי האבחון והטיפול.
לאור זאת, גם הרפואה המסורתית נדרשת להתאים את עצמה ולתרגם עקרונות טיפוליים מסורתיים לשפה קלינית עכשווית.
מעבר לשימוש בחומרי גלם בעלי השפעה פיזיולוגית מובהקת, יש מקום לבחון את ההשפעות האנרגטיות היכולות להועיל. הגורמים למחלה עוד לא ידועים לגמרי ולכן יש קושי במציאת תרופה נכונה. אבל כשמדובר במבוגרים בגיל השלישי, בעלי מנגנונים רגישים יש היענות אנרגטית גבוהה. חקירה והתנסות יכולים להציע כלים חדשים בטיפול במחלות ניווניות והזדקנות.
סוקרת ומתרגמת – ענאל אזולאי
כתיבה, טיפול בטווינה, סטודנטית לנטורופתיה והרבליזם בירושלים.
(1) https://pmc.ncbi.nlm.nih.gov/articles/PMC7478559
Salvia miltiorrhiza improves Alzheimer’s disease
(2) https://www.theguardian.com/society/article/2024/aug/22/uk-health-regulator-rejects-lecanemab-as-treatment-for-alzheimers
UK health regulator rejects lecanemab as treatment for Alzheimer’s
(3) https://www.pnas.org/doi/full/10.1073/pnas.0608332104
The presenilin hypothesis of Alzheimer’s disease: Evidence for a loss-of-function pathogenic mechanism
(4) https://pubmed.ncbi.nlm.nih.gov/39259179
Increases in amyloid-β42 slow cognitive and clinical decline in Alzheimer’s disease trials
by Jesus Abanto, Alok K Dwivedi, Bruno P Imbimbo and Alberto J Espay, 11 September 2024, Brain.
DOI: 10.1093/brain/awae216
מוזמנים לכנס עיוני גדול ומרתק בנושא טיפול בצמחים באמצעות צמחי מרפא באלצהיימר דמנציה ופרקינסון.
לצמחי מרפא יש תפקיד חשוב בהאטת אלצהיימר ודמנציה בגיל השלישי. בעוד מדע הרפואה ממשיך לגלות שמחלת אלצהיימר אינה נובעת רק מהצטברות חלבונים במוח, גישות טיפוליות חדשניות מציעות שילוב של צמחי מרפא, תמיכה בפינוי רעלים דרך מערכת הלימפה, איזון ציר מוח–מעי, וחיזוק מחסום הדם–מוח.
בכנס הקרוב תחשפו למחקרים פורצי דרך, לדרכי טיפול מהרפואה ההרבליסטית ולשיח חיוני בין מדע מודרני וחוכמה מסורתית.
הכנס יתקיים ביום שני 15/9/25 במרכז דוהל, תל אביב.


